ドデカカルボニル三オスミウム
| ドデカカルボニル三オスミウム | |
|---|---|
| |
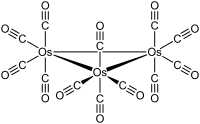
cyclo-tris(tetracarbonylosmium) | |
別称 Osmium carbonyl | |
| 識別情報 | |
| CAS登録番号 | 15696-40-9 |
| 特性 | |
| 化学式 | C12O12Os3 |
| モル質量 | 906.81 g/mol |
| 外観 | 黄色固体 |
| 密度 | 3.48 g/cm3 |
| 融点 |
224 °C, 497 K, 435 °F |
| 沸点 |
真空中で昇華 |
| 水への溶解度 | 不溶 |
| その他の溶媒への溶解度 | 有機溶媒にわずかに可溶 |
| 構造 | |
| 双極子モーメント | 0 D (0 C・m) |
| 危険性 | |
| 主な危険性 | CO source |
| Rフレーズ | 22-36/37/38 |
| Sフレーズ | 22-26-36/37/39 |
| 関連する物質 | |
| 関連物質 | ドデカカルボニル三鉄 ドデカカルボニル三ルテニウム デカカルボニルジヒドリド三オスミウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ドデカカルボニル三オスミウム(Triosmium dodecacarbonyl)は、化学式Os3(CO)12の化合物である。黄色の金属カルボニルクラスター化合物で、有機オスミウム化合物の前駆体として重要である。クラスター化学の進歩の多くは、ドデカカルボニル三オスミウムやその軽いアナログであるドデカカルボニル三ルテニウムの誘導体に由来するものである。
構造と合成
[編集]クラスターはD3h分子対称性を持ち、各々が軸方向に2つ、水平方向に2つのCO配位子を持つオスミウム原子からなる正三角形の形状である。Os-Os結合長は288 pmである[1]。ドデカカルボニル三ルテニウムも同じ構造を持つが、ドデカカルボニル三鉄は異なり、2つの架橋CO配位子がC2v対称となっている。
ドデカカルボニル三オスミウムは、高圧下、175℃で酸化オスミウム(VIII)と一酸化炭素を直接反応させることで得られる[2]。
- 3 OsO4 + 24 CO → Os3(CO)12 + 12 CO2
生成物はほぼ定量的である。
反応
[編集]ドデカカルボニル三オスミウムの化学的性質はかなり調べられている。
クラスターと配位子の直接反応は、しばしば複雑な生成物文分布をもたらす。これは、内部Os-CO結合を壊すには高温が必要であり、そのような高温では、最初に形成された付加物がさらに反応するためである。脱カルボニル剤としてトリメチルアミン-N-オキシドを用いると、Os3(CO)11(MeCN)やOs3(CO)10(MeCN)2等のより不安定な誘導体に変換される[3]。Os3(CO)11(MeCN)は、様々なより弱い塩基性配位子とでも反応して、Os3(CO)11(ethylene)やOs3(CO)11(pyridine)等の付加物を生成する。Os3(CO)12とエチレンやピリジンとの直接反応ではこれらの有機配位子が分解し、ビニルヒドリド(HOs3(CO)10(η1,η2-C2H3))やピリジルヒドリド(HOs3(CO)10(NC5H4))を生成する。これらの生成物は、Os-H結合及びOs-C結合の安定性を示す。
Os3(CO)12は、炭化水素が金属の集合体と相互作用する方法を試験するためのプラットフォームとなる。例えば、CH3(H)Os3(CO)10は、アゴスティック相互作用の最初の明確な例の1つである[4]。
化学結合の観点からは、デカカルボニルジヒドリド三オスミウム(H2Os3(CO)10)は注目に値する。この化合物では、2つのヒドリド配位子が1つのOs-Os間を架橋し、ジボランと似た反応性を示す[5]。
ペンタカルボニルオスミウムは、280-290℃で固体ドデカカルボニル三オスミウムを200気圧の一酸化炭素と反応させることで得られる[6]。
出典
[編集]- ^ Corey, E. R.; Dahl, L. F. "The Molecular and Crystal Structure of Os3(CO)12" Inorganic Chemistry 1962, volume 1, pages 521-526; doi:10.1021/ic50003a016.
- ^ Drake, S. R.; Loveday, P. A. "Dodecarbonyltriosmium" Inorganic Syntheses, 1990, volume 28, pages 230-231. ISBN 0-471-52619-3.
- ^ Nicholls, J. N.; Vargas, M. D. "Some Useful Derivatives of Dodecarbonyltriosmium" Inorganic Syntheses, 1990, volume 28, pages 232-235. ISBN 0-471-52619-3.
- ^ Calvert, R. B.; Shapley, J. R. "Decacarbonyl(methyl)hydrotriosmium: NMR evidence for a Carbon..Hydrogen..Osmium Interaction" Journal of the American Chemical Society 1978, volume 100, pages 7726-7727; doi:10.1021/ja00492a047.
- ^ Keister, J. B.; Shapley, J. R. "Solution Structures and Dynamics of complexes of Decacarbonyldihydrotriosmium with Lewis Bases" Inorganic Chemistry 1982, volume 21, pages 3304-3310; doi:10.1021/ic00139a011.
- ^ Rushman, Paul; Van Buuren, Gilbert N.; Shiralian, Mahmoud; Pomeroy, Roland K. (1983). “Properties of the Pentacarbonyls of Ruthenium and Osmium”. Organometallics 2 (5): 693-94. doi:10.1021/om00077a026.
