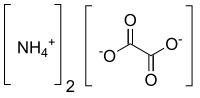
シュウ酸アンモニウム
表示
| シュウ酸アンモニウム | |
|---|---|
| |
Diammonium ethanedioate | |
別称 Diammonium oxalate | |
| 識別情報 | |
| CAS登録番号 | 1113-38-8 |
| PubChem | 14213 |
| ChemSpider | 13577 |
| UNII | 0PB8MO5U0H |
| ChEBI | |
| |
| |
| 特性 | |
| 化学式 | C2H8N2O4 |
| モル質量 | 124.1 g mol−1 |
| 外観 | 白色固体 |
| 融点 |
70 C (158 F, 343.15 K) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
シュウ酸アンモニウムは、アンモニウムのシュウ酸塩(ときに一水和物として)。化学式はC2H8N2O4でより一般的には(NH4)2C2O4と書かれる。通常条件下では無色(白色)の塩であり、無臭で不揮発性である。シュウ酸のアンモニウム塩でもあり、多くの植物や野菜に存在する。
脊椎動物
[編集]グリオキシル酸やアスコルビン酸の代謝により脊椎動物の体内で生成される。これは代謝されずに尿で排泄される[1]。ある種の腎臓結石の成分である[2][3]。グアノにも含まれている。
鉱物学
[編集]オキサマイトは、シュウ酸塩の天然の鉱物形である。この鉱物は非常に珍しい[4]。
化学的性質
[編集]シュウ酸塩アンモニウムは、分析試薬及び一般的な還元剤として使用される[1]。これと他のシュウ酸塩は、体外の血液を保存するための抗凝固剤として使用される。
地球科学
[編集]酸性シュウ酸アンモニウム(シュウ酸でpH 3に酸性化されたシュウ酸アンモニウム)は、結晶性の低い鉱物(フェリハイドライトなど)、鉄(II)含有鉱物(磁鉄鉱など)や有機物から鉄とアルミニウムを抽出するために土壌化学分析で一般的に使用される[5][要ページ番号]。
出典
[編集]- ^ a b National Center for Biotechnology Information. PubChem Compound Database; CID 14213 (accessed 15 November 2016).
- ^ The International Pharmacopoeia, p.1292, Volume 1, World Health Organization, 2006 ISBN 92-4-156301-X.
- ^ N G Coley, "The collateral sciences in the work of Golding Bird (1814-1854)", Medical History, iss.4, vol.13, October 1969, pp.372.
- ^ http://www.mindat.org
- ^ Rayment, George; Lyons, David (2011). Soil Chemical Methods - Australasia. CSIRO Publishing. ISBN 9780643101364
