可溶性グアニル酸シクラーゼ
| 可溶性グアニル酸シクラーゼ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| 識別子 | |||||||||
| EC番号 | 4.6.1.2 | ||||||||
| CAS登録番号 | 9054-75-5 | ||||||||
| 別名 | Guanyl cyclase, Guanylyl cyclase | ||||||||
| データベース | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB構造 | RCSB PDB PDBj PDBe PDBsum | ||||||||
| 遺伝子オントロジー | AmiGO / QuickGO | ||||||||
| |||||||||
可溶性グアニル酸シクラーゼ (Soluble guanylyl cyclase、Soluble guanylate cyclase、sGC)は、一酸化窒素 (NO)の唯一の既知の受容体である。 可溶性で、すなわち完全に細胞内に存在する。 最も注目すべきは、この酵素が血管拡張に関与していることである。 ヒトでは、遺伝子GUCY1A2 、 GUCY1A3 、 GUCY1B2およびGUCY1B3によってエンコードされる。
EC番号4.6.1.2に分類されている [1]。
構造
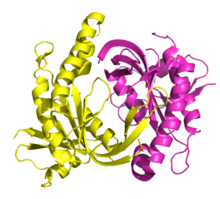
[編集]sGCは、1つのアルファ(1、2)サブユニットと1つのヘム結合ベータ(1、2)サブユニットで構成されるヘテロダイマーである。 各サブユニットは、N末端HNOXドメイン、PAS様ドメイン、コイルドコイルドメイン、C末端触媒ドメインの4つのドメインで構成されている。 哺乳類の酵素は、ベータ1サブユニットのHNOXドメインにある近位ヒスチジンリガンドとともに、二量体あたり1つのヘムを含んでいる。 Fe(II)の形では、このヘム部分は一酸化窒素の標的であり、適切な刺激後に内皮細胞によって合成される。 一酸化窒素がヘムに結合すると、C末端触媒ドメインが活性化され、GTPからcGMPが生成される。
sGCのベータサブユニットのHNOX(ヘム一酸化窒素/酸素結合)ドメインは、補綴ヘムグループを含み、広範囲の生物で見られる関連センサータンパク質のファミリーの一部である。 HNOXドメインは、結合ヘムを使用して、一酸化窒素、酸素、および/またはおそらく一酸化炭素などのガス状リガンドを感知する。 sGCのHNOXドメインには利用可能な構造がないが、いくつかの細菌HNOXドメインが結晶化されている(pdbコード1U55、1XBN、2O09など)。
sGCにはPASタイプの規制ドメイン(regulatory domain)も含まれている。 PASドメインは、それが見つかった最初の3つのタンパク質(周期時計タンパク質、ARNTタンパク質、およびシングルマインドタンパク質)にちなんで名付けられた。光、酸化ストレス、または二原子ガスを含むさまざまな条件のセンサーとしての補綴グループとして働く。 sGCの場合、PASドメインはヘテロダイマーの形成を媒介し、HNOXドメインから触媒グアニル酸シクラーゼドメインへのシグナル伝播に役割を果たす可能性がある。 sGCのPASドメインには利用可能な構造はないが、sGCと高い配列相同性を持つタンパク質のPASドメインは結晶化されている(pdbコード2P04)。
sGCのPASドメインの後には、さまざまなシグナル伝達タンパク質に見られるシグナル伝達ヘリックスと呼ばれるセグメントを含む拡張コイルドコイル領域が続く。 sGCベータサブユニットのコイルドコイル領域の結晶構造が決定された(pdbコード3HLS)。
sGCのC末端にある250残基のグアニル酸シクラーゼドメインは、可溶性および膜結合グアニリルシクラーゼに高度に保存されており、多くのアデニリルシクラーゼの触媒ドメインと重要な相同性を共有している。 2008年に、細菌のグアニル酸シクラーゼドメイン(pdbコード2W01)とsGCグアニル酸シクラーゼ触媒ドメイン(pdbコード3ET6)の最初の構造が報告された。 2009年後半に、ヒトのグアニル酸シクラーゼ触媒ドメイン、ベータサブユニットの結晶構造が報告された(pdbコード2WZ1)。
完全長のsGCの結晶構造はいまだに明らかにされてはいないが、おおよその立体構造は可視化されている[2]。膜結合性と予想されるが、その局在はいまだに不明である[3]。
制御
[編集]NOは、sGC活性の少なくとも200倍の増加につながる。 一酸化窒素は部分的に満たされたpi *軌道を持っているため、バックボンディングはヘムNO複合体の曲がったジオメトリを優先する。 NOには強いトランス効果があり、NO結合が電子を軸配位子に向かってdz2軌道に非局在化させると、ヒスチジンと鉄の結合が弱まる。 このように、遠位の位置で結合している一酸化窒素は、5配位のFe-NO錯体に解離するHis-Fe-NO錯体を与える。 ただし、sGCの活性化における2つの異なる[NO]依存プロセスの同定により、近位のNOがヒスチジンの置換に関与し、中間の6座標のNO-Fe-NO複合体が生じると推測されている。 生成物の濃度に応じて、中間体は2つの5配位型、より活性な遠位NO結合型、または活性の低い近位NO結合型のいずれかに解離する。 対立仮説では、2番目の非ヘム結合部位が2番目のNO依存性活性化プロセスを説明し、完全に活性な酵素を与えるとしている[4]。
酸化ストレス条件下では、Fe(II)sGCは酸化され、ヘムを失う可能性がある。 ヘムフリー(apo-sGC)はもはやNOに反応しないが、いわゆるsGC活性化化合物に反応する。 後者は空のヘムポケットに結合し、NOによるFe(II)sGCの活性化と同様の方法で酵素を活性化する。
さらに、sGCにはアロステリック部位が含まれており、sGC刺激物質が結合する。 それらはNO-sGCシグナル伝達を増強し、NOの準最大活性濃度がsGCの最大活性化に到達するようにする。 単独では、sGC刺激因子はsGCにわずかな影響しか与えない。
薬物ターゲットとして
[編集]2017年2月現在、sGCをターゲットとするFDA承認薬は1つのみである。 リオシグアト (商品名Adempas、アデムパス)は、2種類の肺高血圧症 (PH)、すなわち慢性血栓塞栓性肺高血圧症 (CTEPH)と肺動脈高血圧症 (PAH)を治療する、「sGC刺激薬」という新規クラスの最初の薬剤である[5]。
シナシグアト (BAY 58-2667) はsGC刺激剤で候補薬であったが、急性非代償性心不全の臨床試験で緊急介入を必要とする治療誘発性低血圧イベントの発生率が高いため、有効性を実証できなかった[6] [7]。
ベルイシグアト(英語: Vericiguat、MK-1242、BAY1021189)はsGC刺激剤で、新規経口投与慢性心不全治療剤としてHFrEFのP3試験は2019年8月28日に中止となったが[8]、2019年10月現在HFpEFのP2試験段階にある[9][10](2020年6月1日までの予定)。
出典
[編集]- ^ Soluble guanylyl cyclase - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス
- ^ Melody G. Campbell, Eric S. Underbakke, Clinton S. Potter, Bridget Carragher, and Michael A. Marletta. "Single-particle EM reveals the higher-order domain architecture of soluble guanylate cyclase" PNAS February 25, (2014). 111 (8) 2960-2965. PMID 24516165
- ^ 牧野 龍、一酸化窒素の細胞内受容体,可溶性グアニル酸シクラーゼの構造と機能:ガス状分子に対するヘムセンサー部位の選択的感知機構とヘム鉄の配位構造(総説) Journal of Japanese Biochemical Society 89(3): 414-423 (2017)doi:10.14952/SEIKAGAKU.2017.890414
- ^ “Soluble Guanylyl Cyclase”. Encyclopedia of Molecular Pharmacology. Berlin, Heidelberg: Springer. (2008). pp. 1146–1147. doi:10.1007/978-3-540-38918-7_6754. ISBN 978-3-540-38916-3
- ^ “FDA approves Adempas to treat pulmonary hypertension”. Press Announcements. United States Food and Drug Administration (8 October 2013). 3 February 2017時点のオリジナルよりアーカイブ。2019年10月15日閲覧。
- ^ “Why do drugs for acute heart failure fail?”. European Journal of Heart Failure 14 (9): 955–6. (September 2012). doi:10.1093/eurjhf/hfs122. PMID 22820315.
- ^ “Cinaciguat, a soluble guanylate cyclase activator, unloads the heart but also causes hypotension in acute decompensated heart failure”. European Heart Journal 34 (1): 57–67. (January 2013). doi:10.1093/eurheartj/ehs196. PMID 22778174.
- ^ 左室駆出率が低下した心不全(HFrEF)患者を対象に、経口sGC刺激薬vericiguatの有効性及び安全性を検討する無作為化、並行群間、プラセボ対照、二重盲検、イベント主導型、多施設共同、ピボタル、第III相、臨床アウトカム試験 (VICTORIA) 臨床研究情報ポータルサイト
- ^ “「HFpEF」の新薬開発、SGLT-2阻害剤に期待 心不全治療、エントレストの主要項目未達で”. 日刊薬業(じほう). (2019年10月15日) 2019年10月15日閲覧。
- ^ 左室駆出率が保持された心不全(HFpEF)患者を対象に、日常生活動作での身体機能の改善のためにsGC刺激薬vericiguatを経口投与した際の有効性及び安全性を評価する無作為化、並行群間、プラセボ対照、二重盲検、多施設共同試験臨床研究情報ポータルサイト
