ロイペプチン
表示
| ロイペプチン | |
|---|---|
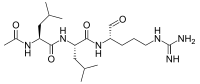
| |
(2S)-5-Guanidino-2-[[N-(N-acetyl-L-leucyl)-L-leucyl]amino]pentanal | |
| 識別情報 | |
| CAS登録番号 | 55123-66-5 |
| PubChem | 72429 |
| ChemSpider | 65357 |
| 日化辞番号 | J438.138F |
| |
| |
| 特性 | |
| 化学式 | C20H38N6O4 |
| モル質量 | 426.55 g mol−1 |
| 精密質量 | 426.295453734 g mol−1 |
| 関連する物質 | |
| 関連するアルカンアミド | グスペリムス |
| 関連物質 | シンタリン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ロイペプチン(leupeptin)は、システイン、セリン、スレオニンペプチダーゼを阻害することができる天然のプロテアーゼ阻害剤である。N-acetyl-L-leucyl-L-leucyl-L-argininalとしても知られている。
ロイペプチンは、特定の酵素反応を研究する際のin vitro実験においてしばしば使用される。これらの研究のために細胞を溶解させた時、プロテアーゼ(多くはリソソームに含まれる)が放出される。これらのプロテアーゼが溶解液中に自由に存在した場合、研究している反応の生成物を破壊してしまい、実験は解釈不能となる。喩えば、ロイペプチンはカルパインの抽出において、カルパインが特定のプロテアーゼによって加水分解されるのを阻害するため使用することができる。推奨濃度は1-10 µM (0.5-5 μg/mL) である。
ロイペプチンは放線菌によって生産される有機化合物である。ロイペプチンはセリンプロテアーゼ(トリプシン〈Ki = 3.5 nM〉、プラスミン〈Ki= 3.4 nM〉、ブタカリクレイン)、システインプロテアーゼ(パパイン、カテプシンB〈Ki = 4.1 nM〉、エンドプロテイナーゼLys-C)を阻害する。α-キモトリプシンあるいはトロンビンは阻害しない。ロイペプチンは競合的遷移状態阻害剤であり、過剰な基質によってその阻害作用は軽減される。
ロイペプチンは水(4 °Cで1週間、 −20 °Cで1カ月間安定)、エタノール、酢酸、DMFに可溶である。
ロイペプチンは中耳ならびに内耳感染に対して局所的に投与される。
脚注
[編集]- ^ RCSB Protein Data Bank. “1JRS Structure Summary”. 2012年9月6日閲覧。
