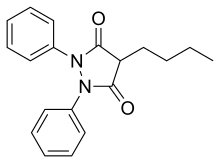
フェニルブタゾン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Butazolidine |
| 法的規制 |
|
| 識別 | |
| CAS番号 |
50-33-9 |
| ATCコード | M01AA01 (WHO) M02AA01 (WHO) |
| PubChem | CID: 4781 |
| IUPHAR/BPS | 7270 |
| DrugBank |
DB00812 |
| ChemSpider |
4617 |
| UNII |
GN5P7K3T8S |
| KEGG |
D00510 |
| ChEBI |
CHEBI:48574 |
| ChEMBL |
CHEMBL101 |
| 化学的データ | |
| 化学式 | C19H20N2O2 |
| 分子量 | 308.374 g/mol |
| |
フェニルブタゾン (Phenylbutazone) は非ステロイド性抗炎症薬の一つで、短期的な鎮痛および動物の解熱に用いられる。 しばしば "bute" と略される[1]。
アメリカ及びイギリスでは、白血球生産の抑制や再生不良性貧血などの重い副作用があるとして、人間には適用されなくなった。馬肉混入問題において、この薬の付着した馬肉が混入した恐れがあるとして調査対象となった。少くとも、イギリスでは一般に陰性の結果が得られている[2]。
適用
[編集]ヒト用
[編集]フェニルブタゾンは、1949年に関節リウマチおよび痛風の治療の為に人間に用いられるようになった。しかし、アセトアミノフェンなどの家庭用鎮痛剤と共に用いると少量でも永続的な肝機能低下をおこし、命に関るケースも多数発生した[要出典]。アメリカでは、もはや人間には用いられず、流通もしていない[3]。イギリスでは、強直性脊椎炎 の治療に用いられるが、他の治療法が適さない場合に限られる[4]。
ウマ用
[編集]アメリカでは、フェニルブタゾンはウマ用の非ステロイド性抗炎症薬としてもっとも広く用いられている[5]。次のように用いられる。
- 鎮痛剤: 感染症や捻挫、オーバーユース傷害、屈腱炎、関節痛、関節炎、蹄葉炎などの筋骨格系障害に際して鎮痛のために用いられる。他の非ステロイド性抗炎症薬と同様、運動器の組織に直接作用して炎症を抑え、炎症による二次傷害を防ぎ、痛みを緩和し、関節可動域を維持する。筋骨格系障害そのものを治癒するわけではなく、疝痛にも効果がある。
- 解熱薬: 発熱をやわらげるために用いられる。解熱効果によって他の症状を隠すことがあるので、獣医師により使用しなければウマが飲食できない、もしくは発熱により回復が妨げられていると診断されない限り用いるべきではない。
競馬におけるフェニルブタゾンの歴史
[編集]1968年のケンタッキーダービーの優勝馬、ダンサーズイメージはレース後の尿検査においてフェニルブタゾン陽性とされたため降着となった。馬主はマサチューセッツの著名な実業家ピーター・フラー、騎手はボビー・ウセリー。ダンサーズイメージはケンタッキーダービーの優勝を取り消された唯一の競走馬である。 フェニルブタゾンは1968年にはアメリカのほとんどの競馬場で使用可能となっていたが、チャーチルダウンズ競馬場ではまだ認められていなかった。
この事件に関しては未だ論争があり、調査が続いている。問題のレースの数週間前、ピーター・フラーは勝利を暗殺された公民権運動家マーティン・ルーサー・キング・ジュニアの未亡人、コレッタ・スコット・キングに捧げており、毀誉褒貶があった。前年には、キングが居住の差別に対して行なった座り込みのため、ダービーは中止になっていた。40年後も、フラーはこのせいでダンサーズイメージが降着とされたのだと考えている[6][7]。
多数の抗議にもかかわらず、優勝はフォワードパスとされた。ケンタッキーダービーの公式ウェブサイトにはダンサーズイメージとフォワードパスの両方が優勝馬として掲載されている。このサイト上のレース動画のコメントでは、チャーチルダウンズ競馬場の優勝馬銘板には1968年の優勝馬としてやはりダンサーズイメージとフォワードパスの両方が刻まれているとされている[8]。
イヌ用
[編集]フェニルブタゾンはイヌ用に慢性痛の長期治療、特に変形性膝関節症に対して用いられることもある。成犬のおよそ20%は変形性膝関節症を罹患しているため、筋骨格痛の抑制は伴侶動物医療の主要分野となっている。非ステロイド性抗炎症薬全般のイヌに対する安全余裕率は小さく、他の非ステロイド性抗炎症薬(エトドラクやカルプロフェン)の方がより一般的に用いられる。非ステロイド性抗炎症薬全般に、ミソプロストール、シメチジン、オメプラゾール、ラニチジン、スクラルファートなどの胃腸保護剤が含まれることが多い。フェニルブタゾンによる長期治療を受けるイヌは、定期的に血液検査と腎機能モニタリングを受けることが推奨される[9]。
イヌに対するフェニルブタゾンの副作用としては、胃潰瘍、骨髄抑制、発疹、不快感、血液疾患、腎臓の血流減少などがあげられる。
ウマにおける用法・用量
[編集]フェニルブタゾンの血漿中半減期は4-8時間なのに対して炎症滲出液中半減期は24時間であり[10]、一日に一回塗布すれば十分だが、一日二回塗布することも多い[5]。適量(一日あたり2.2-4.4 mg/kg)を守れば継続的に使用しても毒性は十分に低いとされる[11]。蹄葉炎のように痛みの酷い場合、倍量が与えられるが継続的に用いると毒性が表われ、極端に多量(一日あたり 15 mg/kg以上)に用いた場合、一週間で死に至る場合がある[12]。
フェニルブタゾンは経口(膏薬や粉薬、飼料添加物として)、あるいは静脈点滴で投与される。筋肉内注射など静脈以外の場所への注射は組織損傷を与える恐れがあり、禁忌である。同じ静脈に継続して注射しても、組織損傷や浮腫を起こすことがある。
フェニルブタゾンは獣医師の処方なしに用いるべきでない。
副作用
[編集]フェニルブタゾンは他の非ステロイド性抗炎症薬と同様の副作用を引き起こす。オーバードーズや長期間の使用により、胃潰瘍、 血液疾患、腎損傷(多くは用量により腎乳頭壊死)、経口投与の場合は口腔病変、内出血などの副作用が表われる [12]。代謝能力が弱い若いウマや病んだウマ、ストレス下のウマにおいて特に顕著に表われる[13]。潰瘍および足や腹の浮腫のため、腸内血中タンパク質が漏洩し、結果として食欲減退、多渇、体重減少、虚弱などの二次症状が表われ、症状が進むと腎不全や死につながる。
フェニルブタゾンとワルファリンやフェンプロクモンなどのビタミンK拮抗体を共用すると、抗凝固作用が増幅されるため禁忌である。他の非ステロイド性抗炎症薬との共用も、腎疾患や肝疾患のあるウマへの使用も避けなければならない。フェニルブタゾンはワルファリンを血漿結合サイトから排除するため、有毒濃度に達すると脳出血の恐れがある。
無顆粒球症のおそれがあるため、フェニルブタゾンの使用中は定期的に血液検査を受けることが望ましい。
妊娠中または子育て中の牝馬への使用は、胚への毒性がありえるため、また仔に臍帯または乳を介して移る可能性があるため注意が必要である。
子馬に対しても使用することがあるが、特に注意が必要である。未成熟な子馬、敗血症の子馬、肝機能または腎機能に懸念のある子馬、下痢のある子馬に対しては注意深い観察が必要である。 オメプラゾール、 シメチジン、スクラルファートなどの胃腸保護剤と共に用いられることが多い。
使用後も血流中に四、五日残るため、高用量の使用を規則違反とみなす馬術団体もある。
国際がん研究機関により、グループ 3、「ヒトに対する発癌性については分類できない」に分類されている。
フェノブタゾン代謝物がヒトに再生不良性貧血をもたらす可能性があるので[14][15]、食用のウマには使用できない。
発癌性調査
[編集]動物に対するフェノブタゾンの発癌性については意見の対立がある。治療に適切な用量では、ヒトに対する発癌性を示す証拠はない。 前川ら (1987) は、二年間にわたって0.125% から 0.25% のフェノブタゾンを含む餌を与えた DONRYU ラットについて、癌の増加はみられなかったとしている[16]。一方で、カリら (1995) はオスのラットに体重あたり 150 から 300 mg/kg のフェニルブタゾンを二年にわたって食べさせ、珍しい型の腎臓癌(100匹中13匹)が見られ、肝臓癌の割合も増加したとしている[17]。テナン (1993) は非変異原性発癌物質のひとつとしてフェノブタゾンを挙げている[18]。カークランドとファウラー (2010) は、DNAへの作用を調べるコンピュータソフトウェアによるとフェニルブタゾンは変異原ではないとしているが[19]、フェノブタゾンがマウスの骨髄細胞の染色体構造を変化させるという報告もある[20]。カークランドとファウラー (2010) はさらに、ヒトにおけるフェノブタゾンの理論的な発癌効果は患者に処方される量が、何らかの効果が発現しうる濃度よりはるかに低い (<1 mM) ために研究することは不可能だとしている[19]。世界保健機関の国際がん研究機関 (IARC) は、1987年にヒトに対する発癌性の証拠は十分でないと結論している[21]。
薬物相互作用
[編集]副腎皮質ホルモンや他の非ステロイド性抗炎症薬などの抗炎症薬は、胃潰瘍を起こしがちで、出血のリスクがある。抗凝血剤、特にクマリン誘導体などと組み合わせると、さらに出血リスクが高まる。肝毒性のある薬との併用は避ける。
フェノブタゾンは、フェニトイン、バルプロ酸、スルホンアミド、スルホニルウレア抗糖尿病薬、バルビツール酸系、プロメタジン、リファンピシン、クロルフェニラミン、ジフェンヒドラミン、ペニシリンGの血中濃度と作用期間に影響することがある[22]。
オーバードーズ
[編集]フェニルブタゾンのオーバードーズは、腎不全、肝損傷、骨髄抑制、胃潰瘍、胃穿孔などにつながる。毒性の初期症状は食欲減退、鬱などである[22]。
化学的性質
[編集]フェニルブタゾンは結晶で、n-ブチルマロン酸ジエチルと1,2-ジフェニルヒドラジンを塩基存在下で乾固させて得られる。この反応はラクタム化による複素環化反応と見ることができる。
フェニルブタゾンの主要な代謝生成物であるオキシフェンブタゾン(4-ブチル-1-(4-ヒドロキシフェニル)-2-フェニル-3,5-ピラゾリジンジオン)は、片方のフェニル基のパラ位の水素がヒドロキシ基に置き換わった点のみ異なる。
出典
[編集]- ^ “Death and Disarray at America's Racetracks”. New York Times (24 March 2012). 2015年11月7日閲覧。
- ^ “Horse meat investigation. Advice for consumers”. Enforcement and regulation. Food Standards Agency. 19 May 2013閲覧。
- ^ “FDA Order Prohibits Extralabel Use of Phenylbutazone in Certain Dairy Cattle”. Food and Drug Administration (2003年2月28日). 2009年9月16日時点のオリジナルよりアーカイブ。2015年11月7日閲覧。
- ^ NHS: Drugs used in Rheumatic Diseases and Gout Archived 2013年4月29日, at the Wayback Machine.
- ^ a b McIlwraith CW, Frisbie DD, Kawcak CE.
- ^ Boston Globe article about the 40th Anniversary of the Race
- ^ “Sports: Dancer's tainted image”. 2007年10月7日閲覧。
- ^ “Kentucky Derby 132” (2006年). 2007年10月7日閲覧。
- ^ “Wedgewood Pharmaceuticals-Phenylbutazol”. 2015年11月7日閲覧。
- ^ Lees P, Taylor KBO, Higgins AJ, Sharma SC. Phenylbuta- zone and oxyphenbutazone distribution into tissue fluids in the horse. J Vet Pharmacol Ther 1986;9:204–212.
- ^ Collins LG, Tyler DE. Phenylbutazone toxicosis in the horse: A clinical study. J Am Vet Med Assoc 1984;184: 699 –703.
- ^ a b MacKay RJ, French TW, Nguyen HT, Mayhew IG.
- ^ Lees P, Higgins AJ. Clinical pharmacology in therapeutic uses of non-steroidal anti-inflammatory drugs in the horse. Equine Vet J 1985;17:83–96.
- ^ Peadar Ó Scanaill. “Phenylbutazone and its availability in ireland – prudent prescribing and dispensing”. Irish Veterinary Journal 63 (12): 766–8. オリジナルの2012年4月2日時点におけるアーカイブ。.
- ^ “Ante and Post-mortem Procedures, Dispositions, Monitoring and Controls - Red Meat Species, Ostriches, Rheas and Emus”. Canadian Food Inspection Agency. 2015年11月7日閲覧。
- ^ Maekawa, Akihiko; Hiroshi Onodera; Hiroyuki Tanigawa; Kyoko Furuta; Jun Kanno; Chiaki Matsuoka; Toshiaki Ogiu; Yuzo Hayashi (1987-01-09). “Long-Term Studies on Carcinogenicity and Promoting Effect of Phenylbutazone in DONRYU Rats”. Journal of the National Cancer Institute 79 (3): 577–584. doi:10.1093/jnci/79.3.577. ISSN 0027-8874 2013年1月24日閲覧。.
- ^ Kari, Frank; John Bucher; Joseph Haseman; Scot Eustis; James Huff (1995). “Long-term Exposure to the Anti-inflammatory Agent Phenylbutazone Induces Kidney Tumors in Rats and Liver Tumors in Mice”. Cancer Science 86 (3): 252–263. doi:10.1111/j.1349-7006.1995.tb03048.x. ISSN 1349-7006 2013年1月24日閲覧。.
- ^ Tennant, R W (October 1993). “A perspective on nonmutagenic mechanisms in carcinogenesis.”. Environmental Health Perspectives 101 (Suppl 3): 231–236. doi:10.1289/ehp.93101s3231. ISSN 0091-6765. PMC 1521175. PMID 8143623.
- ^ a b Kirkland, David; Paul Fowler (2010-01-11). “Further analysis of Ames-negative rodent carcinogens that are only genotoxic in mammalian cells in vitro at concentrations exceeding 1 mM, including retesting of compounds of concern”. Mutagenesis 25 (6): 539–553. doi:10.1093/mutage/geq041. ISSN 0267-8357 2013年1月24日閲覧。.
- ^ Giri, A.K.; A. Mukhopadhyay (1998-12-03). “Mutagenicity assay in Salmonella and in vivo sister chromatid exchange in bone marrow cells of mice for four pyrazolone derivatives”. Mutation Research/Genetic Toxicology and Environmental Mutagenesis 420 (1–3): 15–25. doi:10.1016/S1383-5718(98)00138-7. ISSN 1383-5718 2013年1月24日閲覧。.
- ^ IARC (1987). IARC monographs on the evaluation of the carcinogenic risk of chemicals to man.. International Agency for Research on Cancer. pp. 316
- ^ a b “Phenylbutazol for veterinary use”. Wedgewood Pharmacy. 2015年11月7日閲覧。


