ダブラフェニブ
表示
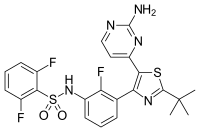 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Tafinlar |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 識別 | |
| CAS番号 | 1195765-45-7 |
| ATCコード | L01XE23 (WHO) |
| PubChem | CID: 44462760 |
| ChemSpider | 25948204 |
| KEGG | D10064 |
| ChEBI | CHEBI:75045 |
| ChEMBL | CHEMBL2028663 |
| 化学的データ | |
| 化学式 | C23H20F3N5O2S2 |
| 分子量 | 519.56 g/mol |
| |
| |
ダブラフェニブ(英語: Dabrafenib)は、BRAF 遺伝子変異陽性癌の治療に用いられる医薬品である。商品名はタフィンラー (Tafinlar) 。細胞増殖を制御するB-Raf酵素の阻害剤として作用する。ダブラフェニブはBRAF (V600) 変異を有する転移性悪性黒色腫への第I相ならびに第II相臨床試験で臨床的有効性と管理可能な安全性プロファイルを示した[1][2]。米国FDAは2013年5月にBRAF V600E変異陽性の進行悪性黒色腫に対する治療薬としてダブラフェニブを承認した[3][4]。開発コードGSK2118436。
臨床試験の結果、6か月から7か月でダブラフェニブおよび他のBRAF阻害薬への抵抗性が生じることが明らかとなった[5]。この抵抗性を克服するため、BRAF V600E/K変異を有する悪性黒色腫の治療に際してダブラフェニブはMEK阻害薬トラメチニブと併用される[5]。2014年1月には、トラメチニブとの併用療法がFDAに迅速承認された[6][7]。また2015年9月には欧州でも悪性黒色腫の併用療法が承認された[8]。
出典
[編集]- ^ Gibney, G. T.; Zager, J. S. (2013). “Clinical development of dabrafenib in BRAF mutant melanoma and other malignancies”. Expert Opinion on Drug Metabolism & Toxicology 9 (7): 1. doi:10.1517/17425255.2013.794220. PMID 23621583.
- ^ Huang, T.; Karsy, M.; Zhuge, J.; Zhong, M.; Liu, D. (2013). “B-Raf and the inhibitors: From bench to bedside”. Journal of Hematology & Oncology 6: 30. doi:10.1186/1756-8722-6-30. PMC 3646677. PMID 23617957.
- ^ “GSK melanoma drugs add to tally of U.S. drug approvals”. Reuters. (May 30, 2013)
- ^ “GSKの2つの経口抗がん薬、BRAF阻害剤Tafinlar(dabrafenib)と初のMEK阻害剤Mekinist™(trametinib)が単剤療法としてFDAの承認を取得”. グラクソ・スミスクライン (2013年6月12日). 2015年4月28日閲覧。
- ^ a b Combined BRAF and MEK Inhibition in Melanoma with BRAF V600 Mutations. 367. New England Journal of Medicine. (November 1, 2012). pp. 1694–703. doi:10.1056/NEJMoa1210093. PMC 3549295. PMID 23020132.
- ^ “Dabrafenib/Trametinib Combination Approved for Advanced Melanoma”. OncLive. (January 9, 2013)
- ^ “GSK、Mekinist(trametinib)とTafinlar(dabrafenib)の併用療法についてFDAから迅速承認を取得”. グラクソ・スミスクライン (2014年1月16日). 2015年4月28日閲覧。
- ^ “ノバルティス、重篤な悪性黒色腫患者さんを対象とした欧州初の併用療法として、ダブラフェニブ/トラメチニブに対するEU承認を取得”. ノバルティス (2015年9月16日). 2015年9月17日閲覧。
