エサキセレノン
表示
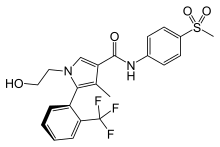 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Minnebro |
| 法的規制 |
|
| 薬物動態データ | |
| 血漿タンパク結合 | ≧98% |
| 代謝 | 酸化、グルクロン酸抱合及び加水分解 |
| 半減期 | 18.6時間 |
| 排泄 | 54.0%が糞中, 38.5%が尿中 |
| データベースID | |
| CAS番号 | 1632006-28-0 |
| PubChem | CID: 25052023 |
| ChemSpider | 28666733 |
| UNII | N62TGJ04A1 |
| KEGG | D10892 |
| ChEMBL | CHEMBL2181932 |
| 別名 | CS-3150; XL-550 |
| 化学的データ | |
| 化学式 | C22H21F3N2O4S |
| 分子量 | 466.48 g·mol−1 |
| |
| |
エサキセレノン(Esaxerenone[1])は、エクセリクシス社が発見し、第一三共が実用化した非ステロイド系抗鉱質コルチコイド薬である。日本では2019年1月に高血圧症の治療薬として承認された[2][3][4][5]。開発コードはCS-3150とXL-550である。アルドステロンの受容体である鉱質コルチコイド受容体(MR)に対して高選択的完全遮断薬として作用する。2019年1月時点で、糖尿病性腎症を対象とした第III相臨床試験が行われている[3]。
効能・効果
[編集]- 高血圧症[6]
禁忌
[編集]エサキセレノンは、次の患者には禁忌である[6]。
- 製剤成分に対し過敏症の既往歴のある患者
- 高カリウム血症の患者もしくは本剤投与開始時に血清カリウム値が5.0mEq/Lを超えている患者
- 重度の腎機能障害(eGFR 30mL/min/1.73m2未満)のある患者
- カリウム保持性利尿剤(スピロノラクトン、トリアムテレン、カンレノ酸カリウム)、アルドステロン拮抗剤(エプレレノン)またはカリウム製剤(塩化カリウム、グルコン酸カリウム、アスパラギン酸カリウム、ヨウ化カリウム、酢酸カリウム)を投与中の患者
副作用
[編集]重大な副作用として、高カリウム血症(1.7%)が知られている[6]。
薬物動態
[編集]吸収
[編集]エサキセレノンの生物学的利用率は89%である[6]。
分布
[編集]エサキセレノン内服後3時間で血中濃度は最高値に達し、半減期は18.6時間である[6]。血中における血漿タンパク結合率は98%以上である[6]。
代謝
[編集]主な代謝物は、O-グルクロン酸抱合体またはアミド結合加水分解物のグルクロン酸抱合体である[6]。その他、CYP3A4とCYP3A5で酸化される[6]。
排泄
[編集]投与後288時間迄に、糞中に54.0%、尿中に38.5%が排泄された[6]。
鉱質コルチコイド受容体選択性
[編集]鉱質コルチコイド受容体に対する親和性は既存の鉱質コルチコイド受容体拮抗薬より高く、スピロノラクトンの4倍、エプレレノンの76倍に達する[3][4][5]。
一方で、糖質コルチコイド受容体、アンドロゲン受容体、プロゲステロン受容体には親和性を持たない[7]:57[8]。
関連項目
[編集]参考資料
[編集]- ^ last, First Middle (2017-09-23). STI Product Title - Phase 2; SBIR, UNL -- edit edit edit. doi:10.2172/1395716.
- ^ “「ミネブロ®錠」の高血圧症に係る国内製造販売承認取得のお知らせ - プレスリリース - 報道関係者の皆さま - 第一三共株式会社”. www.daiichisankyo.co.jp. 2021年8月27日閲覧。
- ^ a b c http://adisinsight.springer.com/drugs/800021527
- ^ a b “Mineralocorticoid receptor antagonists-pharmacodynamics and pharmacokinetic differences”. Curr Opin Pharmacol 27: 78–85. (2016). doi:10.1016/j.coph.2016.02.005. PMID 26939027.
- ^ a b “Nonsteroidal antagonists of the mineralocorticoid receptor”. Curr. Opin. Nephrol. Hypertens. 24 (5): 417–24. (2015). doi:10.1097/MNH.0000000000000147. PMID 26083526.
- ^ a b c d e f g h i “ミネブロ錠1.25mg/ミネブロ錠2.5mg/ミネブロ錠5mg 添付文書”. www.info.pmda.go.jp. PMDA. 2021年8月27日閲覧。
- ^ “ミネブロ錠1.25mg/ミネブロ錠2.5mg/ミネブロ錠5mg インタビューフォーム”. www.info.pmda.go.jp. PMDA. 2021年8月27日閲覧。
- ^ Arai, Kiyoshi; Homma, Tsuyoshi; Morikawa, Yuka; Ubukata, Naoko; Tsuruoka, Hiyoyuki; Aoki, Kazumasa; Ishikawa, Hirokazu; Mizuno, Makoto et al. (2015-08-15). “Pharmacological profile of CS-3150, a novel, highly potent and selective non-steroidal mineralocorticoid receptor antagonist”. European Journal of Pharmacology 761: 226–234. doi:10.1016/j.ejphar.2015.06.015. ISSN 1879-0712. PMID 26073023.
