フェニルアラニン
| フェニルアラニン | |
|---|---|

| |

| |
Phenylalanine | |
別称 2-Amino-3-phenylpropanoic acid | |
| 識別情報 | |
| CAS登録番号 | 150-30-1 (DL) |
| PubChem | 994 |
| ChemSpider | 5910 |
| UNII | 8P946UF12S |
| DrugBank | DB00120 |
| KEGG | D00021 |
| ChEMBL | CHEMBL301523 |
| |
| |
| 特性 | |
| 化学式 | C9H11NO2 |
| モル質量 | 165.19g/mol |
| 融点 |
283 度 |
| 沸点 |
295 度 |
| 酸解離定数 pKa | 1.83 (カルボキシル基), 9.13 (アミノ基)[1] |
| 危険性 | |
| NFPA 704 | |
| 引火点 | なし |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
フェニルアラニン (phenylalanine) はアミノ酸の一種で、側鎖にベンジル基を持つ。略号は Phe または F。アラニンの側鎖の水素原子が1つフェニル基で置き換えられた構造を持つことが名称の由来である。室温では白色の粉末性固体である。
性質
[編集]タンパク質構成アミノ酸で、牛乳、卵、肉などの食品中のたんぱく質に多く含まれている必須アミノ酸の1つ。非極性側鎖アミノ酸で、芳香族アミノ酸。糖原性を持つ。
他のアミノ酸と同じく、D体とL体の2つのエナンチオマーを持つ。L-フェニルアラニン (LPA) は天然に存在する化合物であり、DNAによってコードされ、タンパク質を構成する。D-フェニルアラニン (DPA) は化学合成によって人工的に作り出される化合物である。
L-フェニルアラニンは生体内で L-チロシンに変換され、さらに L-ドーパとなる。これがさらにドーパミンやノルアドレナリン、アドレナリンへと誘導される。D-フェニルアラニンはフェネチルアミンに変換されるのみである。
8万人に1人と言われるフェニルケトン尿症では、このフェニルアラニンをチロシンに変化させる酵素、フェニルアラニン-4-モノオキシゲナーゼ (EC 1.14.16.1) の遺伝子の完全欠損により、血中にフェニルアラニンが異常に蓄積される。そのためフェニルアラニンの摂取を控えねばならない。シュガーレスガムなど多くの食品に含まれ、「フェニルアラニンを含む」旨の注意書きが表示されている。実際にはフェニルアラニンそのものが添加されているわけではなく、体内で分解されてフェニルアラニンを生成させる化合物を含む場合にこの表示が付される。例えば甘味料のアスパルテームは加水分解によってフェニルアラニン、アスパラギン酸、メタノールとなる。
コドンの中ではフェニルアラニンのものが最初に発見された。マーシャル・ニーレンバーグ (Marshall Warren Nirenberg) が発見者である。連続したウラシルからなる mRNA をバクテリア E. coli に挿入すると、そのバクテリアはフェニルアラニンのみを繰り返し単位とする新規なタンパク質を生産することを見出した。
フェニルアラニンは血液脳関門を通過する際にトリプトファンと同じチャネルを使用しており、大量に存在するとセロトニンの生成を阻害する。
合成によって作り出されるラセミ体の DL-フェニルアラニン (DLPA) はサプリメントとして利用される。DLPA は慢性疼痛やうつ病、あるいは月経前症候群による情緒不安定に有効な場合があるとされる。また、ADHD(注意欠陥多動性障害)の発症者の活力や注意力・集中力を増進させるという調査結果がある。
生合成
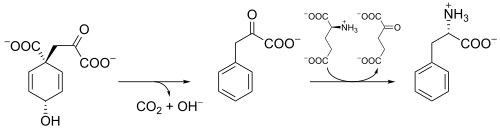
[編集]動物はフェニルアラニンを体内で作り出すことができないため、食物から摂取する必要がある。植物や大部分の微生物においてはシキミ酸経路によってプレフェン酸から生合成される。
プレフェン酸が脱炭酸されると同時にヒドロキシ基を失い、フェニルピルビン酸となる。これがグルタミン酸を窒素源とするアミノ基転移を受け、フェニルアラニンと α-ケトグルタル酸を与える。
出典
[編集]- ^ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
外部リンク
[編集]- フェニルアラニン - 素材情報データベース<有効性情報>(国立健康・栄養研究所)