ビフェニレン
| Biphenylene | |
|---|---|

| |
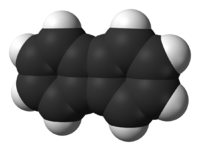
| |
別称 Diphenylene | |
| 識別情報 | |
| CAS登録番号 | 259-79-0 |
| PubChem | 9214 |
| ChemSpider | 8859 |
| UNII | 0Z64I7D5M2 |
| ChEBI | |
| |
| |
| 特性 | |
| 化学式 | C12H8 |
| モル質量 | 152.19 g mol−1 |
| 外観 | Solid |
| 融点 |
109 - 111 °C |
| 関連する物質 | |
| 関連する不飽和炭化水素 | ベンゼン シクロブテン シクロブタジエン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ビフェニレン(biphenylene)は、2つのベンゼン環が、2本の炭素-炭素結合を介して直結した三環式有機化合物である。この2つのベンゼン環が4員環によって連結されている構造のために特殊な性質を示す。
構造が類似したビフェニルは、2つのベンゼン環が1本のC-C単結合を介して直結した、異なる有機化合物である。
平面構造
[編集]ベンゼン環の6個の炭素原子が、平面的に並んでいる事は、よく知られている。ビフェニレンの場合は、分子全体が平面的な構造をしている[2]。基本的に単結合は自由に回転できる結合様式ながら、ビフェニレンの場合は2本の単結合でベンゼン環が結ばれているため、2つのベンゼン環の合計12個の炭素原子は、基本的に同一平面上に並ぶ。
ビフェニルの場合は、2つのベンゼン環が1本のC-C単結合しているだけなので、この単結合を軸にして2つのベンゼン環は自由に回転できるため、2つのベンゼン環の合計12個の炭素原子が、同一平面上の並ぶとは限らない。
原子間の結合と、その性質
[編集]
分光学的ならびに化学的特性は中央の [4n] 環の影響を示す。このことから、その弱まった芳香族性の度合いの観点からこの系に大きな関心が寄せられた。そして、単結合と二重結合が交互にならんでいること、環電流に関する疑問について繰り返し調べられてきた。X線回折を利用した研究で、ベンゼン環のような2つの6員環が結合している炭素原子と炭素原子の結合距離が0.1524 nmであることが示された。これはπ電子系から予想されるより異常な程長い[3][注釈 1]。さらに、電子線回折による研究でも、同様の結果が得られた[4]。
2つの6員間が隔てられていることはNMR置換基効果が中央の [4n] 環を介して伝達されないことによっても反映されている。しかし、敏感なNMRデータ、特にプロトンの共鳴の高磁場シフトは、中央の [4n] 環における電子の非局在化の存在を示している[5][6]。この高磁場シフトは、中央の [4n] 環に常磁性環電流があること、またはないことで、ベンゼノイドの環電流が減少するという観点から解釈されてきた。
磁化率の測定は、相当する純粋な [4n+2] 系と比較して、反磁性磁化率昇高と反磁性異方性がいずれも減少していることを示しており、これは環電流反磁性の低下とも一致する[7][8]。
加えて、気相のビフェニレンの分子軌道のHOMOの結合エネルギーは、7.8 eVである[9]。なお、芳香族性を持つためには、基本的に芳香環を構成している原子が同一平面上に位置するという条件が必要である。その点はビフェニレンも満たしている。しかし、6員環の部分が見せた種々の計測結果は、この部分が反芳香族であると示している[注釈 2]。
反芳香族性
[編集]ビフェニレンが、芳香族である2つのベンゼン環が、4員環で連結された結果、反芳香族性を示している証拠は、他にも存在する[10][11][12][13][14]。
一般にアヌレンはπ電子の数が4n+2個の場合に芳香族性を持つのに対して、π電子の数が4n個の場合は芳香族ではない[注釈 3]。ところが、特殊な構造のためにビフェニレンの場合は、芳香族性を持つはずの6員環の部分は不安定化している。逆に、元来は非常に不安定であるはずの4員環の部分が、幾分安定化している。その度合いは、約1 eVに達する[15][16][17]。
合成
[編集]ビフェニレンの合成は、1941年にW. C. Lothropが成功したと報告した[18]。
ビフェニレン構造は、反応性の高いベンザイン中間体の2量体として理解することもできる[19]。

脚注
[編集]注釈
[編集]- ^ 通常の炭素と炭素の単結合の場合の結合距離は約0.154 nm、ベンゼン環をの6員環を構成している炭素同士の結合の場合の結合距離は約0.139 nm、炭素と炭素の二重結合の場合の結合距離は約0.134 nmである。炭素と炭素の三重結合の場合の結合距離は約0.120 nmである。
- ^ ある環式化合物が有するπ電子と、対応する、同数のπ電子を有している鎖状化合物を比較した際に、それぞれのπ電子のエネルギーを比較した場合の分類である。この比較を行った際に、芳香族(aromatic)のπ電子のエネルギーは、鎖状の化合物と比べて低いために、環状の化合物が安定である。非芳香族(nonaromatic)の場合は、π電子のエネルギーに、鎖状と環状とで差が無い場合である。そして、反芳香族(antiaromatic)のπ電子のエネルギーは、鎖状の化合物と比べて高い。
- ^ ただし、構造が歪むために平面的な分子構造にならないなどの理由で、例外も存在する。なお、アヌレンとは、その分子をケクレ構造式で描いた場合に、単結合と二重結合とが炭素間で交互に並んでいる環状の炭化水素の総称である。
出典
[編集]- ^ “Front Matter”. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. (2014). p. 209. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4
- ^ Waser, Jurg; Lu, Chia-Si (1944). “The Crystal Structure of Biphenylene”. J. Am. Chem. Soc. 66 (12): 2035–2042. doi:10.1021/ja01240a012.
- ^ Fawcett, J. K.; Trotter, J. (1966). “A refinement of the structure of biphenylene”. Acta Crystallogr. 20: 87–93. doi:10.1107/s0365110x66000161.
- ^ Yokozeki, A.; Wilcox Jr., C. F.; Bauer, S. H. (1974). “Biphenylene. Internuclear distances and their root mean square amplitudes of vibration”. J. Am. Chem. Soc. 96 (4): 1026–1032. doi:10.1021/ja00811a014.
- ^ Katritzky, A. R.; Reavill, R. E. (1964). “Nuclear magnetic resonance evidence for partial bond fixation in biphenylene”. Recl. Trav. Chim. Pays-Bas 83 (12): 1230–1232. doi:10.1002/recl.19640831203.
- ^ Fraenkel, G.; Asahi, Y.; Mitchell, M. J.; Cava, M. P. (1964). “NMR spectroscopy of benzocyclobutene and biphenylene”. Tetrahedron 20 (5): 1179–1184. doi:10.1016/s0040-4020(01)98985-9.
- ^ Dauben Jr., Hyp. J.; Wilson, James D.; Laity, John L. (1969). “Diamagnetic susceptibility exaltation in hydrocarbons”. J. Am. Chem. Soc. 91 (8): 1991–1998. doi:10.1021/ja01036a022.
- ^ Anet, F. A. L.; Schenck, G. (1971). “Application of solvent effects to the study of diamagnetic and paramagnetic ring currents”. J. Am. Chem. Soc. 93 (2): 556–557. doi:10.1021/ja00731a061.
- ^ Lüder, Johann; de Simone, Monica; Totani, Roberta (2015). “The electronic characterization of biphenylene—Experimental and theoretical insights from core and valence level spectroscopy”. J. Chem. Phys. 142 (7): 074305. Bibcode: 2015JChPh.142g4305L. doi:10.1063/1.4907723. hdl:11368/2842819. PMID 25702013.
- ^ Wilcox Jr., Charles F.; Uetrecht, J. P.; Grohman, K. K. (1972). “Cycloocta[def]biphenylene”. J. Am. Chem. Soc. 94 (7): 2532. doi:10.1021/ja00762a068.
- ^ Wilcox Jr., Charles F.; Farley, Erik N. (1983). “Dicycloocta[1,2,3,4-def:1',2',3',4'-jkl]biphenylene. Benzenoid Atropism in a Highly Antiaromatic Polycycle”. J. Am. Chem. Soc. 105 (24): 7191–7192. doi:10.1021/ja00362a040.
- ^ Wilcox Jr., Charles F.; Farley, Erik N. (1984). “Dicyclooctabiphenylene. Synthesis and Properties”. J. Am. Chem. Soc. 106 (23): 7195–7200. doi:10.1021/ja00335a055.
- ^ Wilcox Jr., Charles F.; Farley, Erik N. (1985). “Cyclooctannelated Biphenylenes. Diagnosis of an Anomalous Bond Length by Analysis of Ring Current Geometric Factors”. J. Org. Chem. 50 (3): 351–356. doi:10.1021/jo00203a013.
- ^ Farley, Erik Neil (1984). Dicyclooctabiphenylenes (Thesis). Cornell University.
- ^ G. Brunetto, P. A. S. Autreto, L. D. Machado, B. I. Santos, R. P. B. dos Santos, and D. S. Galvao (2012). “Nonzero gap two-dimensional carbon allotrope from porous graphene”. J. Phys. Chem. C 116 (23): 12810–12813. arXiv:1205.6838. Bibcode: 2012arXiv1205.6838B. doi:10.1021/jp211300n.
- ^ Lüder J., Puglia C., Ottosson H., Eriksson O., Sanyal B., Brena B. (2016). “Many-body effects and excitonic features in 2D biphenylene carbon”. J. Chem. Phys. 144 (2): 024702. Bibcode: 2016JChPh.144b4702L. doi:10.1063/1.4939273. PMID 26772582.
- ^ Zhu L., Jin Y.,Xue Q., Li X., Zheng H., Wu T. Ling C. (2016). “Theoretical study of a tunable and strain-controlled nanoporous graphenylene membrane for multifunctional gas separation”. J. Mater. Chem. A 4 (39): 15015–15021. doi:10.1039/C6TA04456E.
- ^ Lothrop, W. C. (1941). “Biphenylene”. J. Am. Chem. Soc. 63 (5): 1187–1191. doi:10.1021/ja01850a007.
- ^ Logullo, Francis M.; Seitz, Arnold M.; Friedman, Lester (1968). "Benzenediazonium-2-Carboxylate and Biphenylene (Benzenediazonium, o-carboxy-, hydroxide, inner salt)" . Organic Syntheses. 48: 12. [https://doi.org/10.15227%2Forgsyn.048.0012 doi:10.15227/orgsyn.048.0012 .; Collective Volume, 5, p. 54
- ^ Campbell, C.D.; Rees, C.W. (1969). “Reactive intermediates. Part I. Synthesis and oxidation of 1- and 2-aminobenzotriazole”. J. Chem. Soc. C 1969 (5): 742–747. doi:10.1039/J39690000742.
