ヒドロン
| ヒドロン | |
|---|---|

| |
| 識別情報 | |
| CAS登録番号 | 12408-02-5 |
| PubChem | 1038 |
| ChemSpider | 1010 |
| KEGG | C00080 |
| ChEBI | |
| |
| 特性 | |
| 化学式 | H+ |
| モル質量 | 1.00739 g mol-1 |
| 精密質量 | 1.007276466812(90) g mol-1 |
| 熱化学 | |
| 標準モルエントロピー S |
108.95 J K-1 mol-1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ヒドロン(Hydron)は、H+という記号で表される、水素原子の陽イオンの一般名である。
概要
[編集]「プロトン」という言葉は、最も多い同位体である軽水素の陽イオンを意味する。「ヒドロン」は、その同位体組成に関わらない陽イオンを表す。そのため、プロトン(1H+)、デューテロン(2H+, D+)、三重水素(3H+, T+)を含む名称である。他のイオンと異なり、ヒドロンは裸の原子核のみから構成される。
ヒドロン(裸の水素原子核)は、反応性が高すぎるため多くの液体中では存在できない。自由なヒドロンは、液体中で分子と反応し、より複雑な陽イオンを形成する。例としては、水中における水素イオンの水和型であるヒドロニウムイオン(H3O+)や最も強い超酸であるフルオロアンチモン酸の不安定な陽イオンH2+がある。このため液体中では、ヒドロンは複雑なイオンと接触して、グロッタス機構により拡散する[2]。水中においてヒドロニウムイオンは、スヴァンテ・アレニウスによる酸の定義の鍵となる。
他の水和型には、1つのプロトンと2つの水分子からなるズンデルカチオン(H5O2+)や1つのプロトンと3つの水分子からなるアイゲンカチオン(H9O4+)があり、グロッタス機構に従う「水素ホッピング」において重要な役割を担っている。ヒドロン自体も、より一般的なブレンステッド-ローリーの酸塩基理論において重要な役割を果たしている。
陰電荷を持つヒドロンのカウンターパートは、ヒドリド(H-)という。
ヒドロンの同位体
[編集]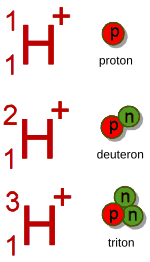
他の水素の同位体は、不安定すぎて意味を持たない。
用語の歴史
[編集]「ヒドロン」(Hydron)という用語は、国際純正・応用化学連合により、未分画の天然の水素同位体混合物に含まれる軽水素、重水素、三重水素について区別がなされないときに「プロトン」に代わる言葉として使うことが勧告されている。「プロトン」という用語は、同位体分離された純粋な1H+を表す[3]。一方、水素化物イオンも存在するために、ヒドロンを単に「水素イオン」(hydrogen ion)ということは推奨されない[4]。
「ヒドロン」という用語は、1988年に国際純正・応用化学連合によって定義された[5][6]。しかし、今でも「ヒドロン」という用語の代わりに「プロトン」という用語が用いられており、プロトン化、脱プロトン化、プロトンポンプ、プロトンチャネル等という用語がある。また酸塩基反応によるH+の移動は、通常は「プロトン移動」と呼ばれる。「ヒドロン」という用語は、速度論的同位体効果や同位体標識等、水素の同位体を区別することが重要な文脈でのみ用いられている。
しかし、天然の水素原子核の99.9844%はプロトンであり、残り(海水では156 ppm)がデューテロン、ごく少量がトリトンである。
関連項目
[編集]出典
[編集]- ^ a b “hydron (CHEBI:15378)”. Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute. 2014年9月5日閲覧。
- ^ [1] Computer modeling of proton-hopping in superacids.
- ^ Nomenclature of Inorganic Chemistry-IUPAC Recommendations 2005 Red Book 2005.pdf IR-3.3.2, p.48
- ^ Compendium of Chemical Terminology, 2nd edition McNaught, A.D. and Wilkinson, A. Blackwell Science, 1997 [ISBN 0-86542-684-8], also online Archived 2005年12月12日, at the Wayback Machine.
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). オンライン版: (2006-) "hydron".
- ^ Bunnet, J.F.; Jones, R.A.Y. (1968). “Names for hydrogen atoms, ions, and groups, and for reactions involving them (Recommendations 1988)”. Pure Appl. Chem. 60 (7): 1115–6. doi:10.1351/pac198860071115.



